ГРАФИТ
ГРАФИТ, минерал из класе самородних елемената угљеничког састава, карактеристичне тамносиве до црне боје и тамносивог огреба. Непровидан, металичног сјаја, савршене цепљивости. Добар проводник електрицитета и топлоте. Релативне тврдине 1--2 по Мосовој скали, специфичне масе 2,2. Кристалише хексагонално и карактерише се типично слојевитом структуром. Јавља се у кристалима табличастог, ређе бипирамидалног хабитуса. Чини листасте до љуспасте или масивне, зрнасте и земљасте агрегате. Настаје магматски, регионално и контактно метаморфно, ређе пегматитски или хидротермално. Има га и у неким метеоритима. Значајније количине г. образоване су регионалним метаморфизмом у форми тзв. графитичних шкриљаца. У овом случају г. настаје редукцијом органске материје која се налази у седиментним стенама. Са интензитетом метаморфизма задобија све уређенију структуру и правилнију грађу. У природи се запажају сви прелази од нискометаморфног, тзв. „аморфног г." до високотемпературног, званог „кристални г". Има широку примену у разним индустријским гранама. Употребљава се у индустрији писаћег прибора, у производњи батерија, за израду контакта у електричним моторима, као лубрикант итд. Захваљујући високој тачки топљења користи се за израду г. лонаца у хемијској индустрији и металургији, као и за израду рефракторних материјала који могу да издрже високе температуре. Добија се и синтетички. У Србији се јавља у Доњој Љубати недалеко од Босиљграда, селу Вети у околини Беле Паланке и на планинама Пасјачи и Јастребцу.
Александар Пачевски
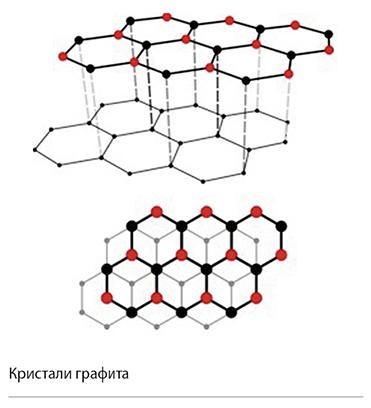
Кристали г. састоје се од бесконачних слогова кондензованих бензенских језгара, без атома водоника на периферији (тзв. графен). Унутар слога, прва и трећа графитна плочица (графен) имају исту оријентацију, док су друга, четврта итд. мало померене. Обе слике приказују положај првог и другог графена. Дуж графитних плочица г. добро проводи електричну струју, слично металима, због електрона који се лако делокализују. Међутим, у смеру вертикалном на плочице (графене), због великог растојања између њих, електрична проводљивост је слаба. Захваљујући својој бензеноидној, поликондензованој структури, г. показује знатну хемијску и термичку стабилност. Иако се састоји од чистог угљеника, са кисеоником у приметној мери реагује тек на око 600 оC, тако да се у одсуству ваздуха може загревати преко 2.000 оC (омекшава изнад 2.500 оC, а топи се тек на 3.750 оC).
У праисторијско време је широко коришћен за украшавање керамичких судова, а касније, у гвоздено доба и за појачање ватросталности судова. После сеобе народа већу примену је поново стекао тек у раном средњем веку код словенских народа у источној и средњој Европи. Највећи произвођачи г. су Кина, Бразил и Индија. Производња природног г. 2014. је била 1,1 мил. т. Врло велика количина производи се синтетички (Немачка, Велика Британија). Близу половине количине ситетичког г. користи се за израду електрода за металургију. Укупна потражња за г. расте око 6% годишње. После Чернобилске нуклеарне катастрофе смањује се његова примена у нуклеарним реакторима. Засад је г. незаменљив у многим новим материјалима и у нанотехнологији.
Петар А. Пфенд
ЛИТЕРАТУРА: М. Арсенијевић, „Графит планине Пасјаче", ГАБП, 1953, XXI; М. Илић, С. Карамата, Специјална минералогија -- први део, Бг 1978; М. Ерцеговац, Р. Томанец, „Графитоиди из метаморфита Доње Љубате (Босиљград)", ГАБП, 1995, LIX, 2; С. Јањић, П. Ристић, Минералогија, Бг 1995; Ullmann's Encyclopedia of Industrial Chemistry Berlin 2002; Д. Бабич, Минералогија, Бг 2003; H. A. Taylor, „Graphite", у: Industrial Minerals and Rocks, Littleton 2005.
*Текст је објављен у 1. књизи III тома Српске енциклопедије (2018)
